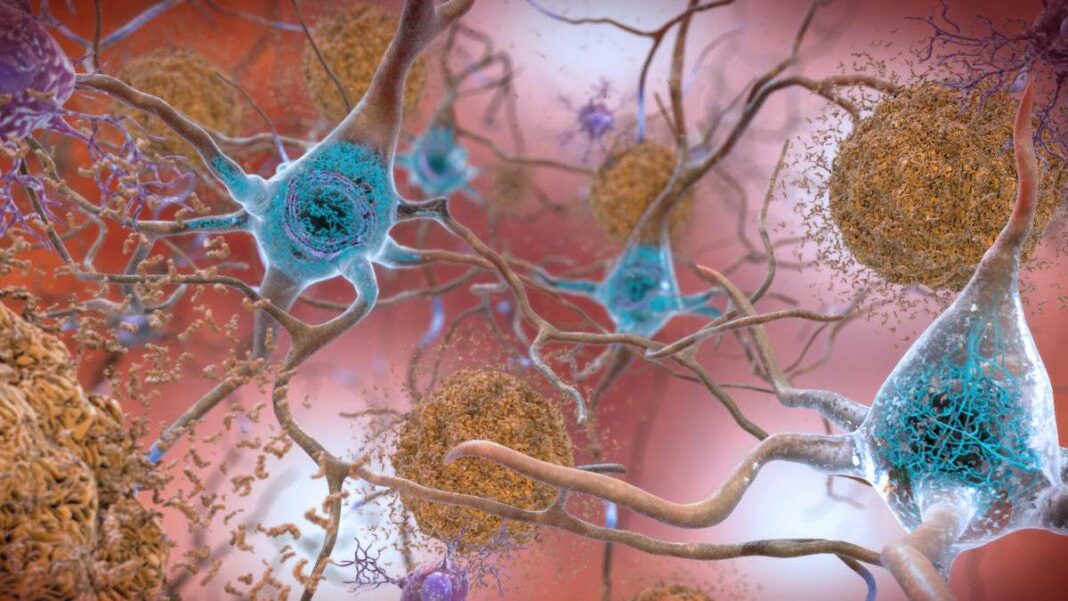
Η νόσος Alzheimer αποτελεί τη συχνότερη αιτία άνοιας στην τρίτη ηλικία. Άλλα μορφές άνοιας είναι η αγγειακή άνοια, η άνοια με σωμάτια Lewy και η μετωποκροταφική άνοια.
Μία ομάδα ερευνητών από τη Γερμανία κατάφερε να ανακλύψει ένα μηχανισμό φλεγμονής που φαίνεται ότι παίζει σημαντικό ρόλο στο σχηματισμό των τοξικών πρωτεϊνών ταυ στον εγκέφαλο των ασθενών με νόσο Alzheimer.
Ο μηχανισμός αυτός αφορά το πρωτεϊνικό σύμπλεγμα γνωστό ως φλεγμονόσωμα NLRP3.
Προηγούμενες έρευνες είχαν αναδείξει το ρόλο του μορίου αυτού στην παραγωγή φλεγμονωδών ουσιών από τα ανοσιακά κύτταρα του εγκεφάλου.
Στη νέα τους έρευνα, οι επιστήμονες από το German Center for Neurodegenerative Diseases (DZNE) και το Πανεπιστήμιο του Bonn στη Γερμανία αποφάσισαν να εξετάσουν το ρόλο του φλεγμονοσώματος NLRP3 στη νόσο Alzheimer και τη μετωποκροταφική άνοια.
Οι ερευνητές εξέτασαν δείγματα νεκροψίας εγκεφάλου από ασθενείς με ή χωρίς μετωποκροταφική άνοια. Εξέτασαν επίσης καλλιέργειες εγκεφαλικών κυττάρων και ποντίκια με χαρακτηριστικές βλάβες που παραπέμπουν σε νόσο Alzheimer και μετωποκροταφική άνοια.
Επικεφαλής της έρευνας ήταν ο Michael T. Heneka, καθηγητής στο Πανεπιστήμιο του Bonn και διευθυντής του Τμήματος Νευροεκφυλιστικών Νόσων και Γεροντοψυχιατρικής.
Ο Heneka ήταν επίσης ο συγγραφέας του άρθρου για τα αποτελέσματα της έρευνας που δημοσιεύτηκε στο επιστημονικό περιοδικό Nature.
Στο άρθρο αυτό, ο Heneka και οι συνεργάτες του περιγράφουν τον τρόπο που σχηματίζονται οι πρωτεΐνες ταυ υπό την επήρεια των φλεγμονωδών διεργασιών από το ανοσοποιητικό σύστημα του εγκεφάλου.
Μία από τις λειτουργίες των πρωτεϊνών ταυ στον υγιή εγκέφαλο είναι η σταθεροποίηση των νευρικών κυττάρων ή νευρώνων.
Ωστόσο, στους ασθενείς με νόσο Alzheimer ή μετωποκροταφική άνοια, οι πρωτεΐνες ταυ υφίστανται χημικές αλλαγές που τις απομακρύνουν από τον κυτταρικό σκελετό και τις κάνουν να προσκολλώνται μεταξύ τους. Χωρίς τη μηχανική σταθερότητα που προσφέρουν οι πρωτεΐνες, το κύτταρο τελικά καταστρέφεται.
Υπερφωσφορυλίωση
Αυτό που κάνει τις πρωτεΐνες ταυ να αποκολλώνται από τις κυτταρικές δομές και να ενώνονται μεταξύ τους είναι μία διαδικασία γνωστή ως υπερφωσφορυλίωση. Η τελευταία αλλάζει τη χημική σύνθεση και τη συμπεριφορά των πρωτεϊνικών μορίων.
Η φωσφορυλίωση αποτελεί σημαντικό ρυθμιστή της πρωτεϊνικής δραστηριότητας των κυττάρων. Περιλαμβάνει προσθήκη και αφαίρεση φωσφορικών ομάδων (PO4) στο πρωτεϊνικό μόριο.
Με τον όρο «υπερφωσφορυλίωση» εννούμε ότι το πρωτεϊνικό μόριο παρουσιάζει κορεσμό από επιπλέον φωσφορικές ομάδες. Στην κατάσταση αυτή, η πρωτεΐνη συμπεριφέρεται με πολύ διαφορετικό τρόπο σε σχέση με το φυσιολογικό.
Οι παρατηρήσεις της νέας έρευνας δείχνουν ότι το φλεγμονόσωμα NLRP3 ενεργοποιεί τα ένζυμα που προκαλούν κορεσμό με φωσφορικά στις πρωτεΐνες ταυ σε βαθμό που αποκολλούνται από τον κυτταρικό σκελετό και σχηματίζουν συσσωματώματα.
«Φαίνεται ότι οι φλεγμονώδεις διαδικασίες που μεσολαβούνται από το φλεγμονόσωμα έχουν μεγάλη σημασία στις περισσότερες, αν όχι σε όλες, τις νευροεκφυλιστικές νόσους που σχετίζονται με παθολογική συμπεριφορά της ταυ», είπε ο Heneka.
Όπως τόνισε, ο μηχανισμός αυτός είναι ιδιαίτερα σημαντικός στη νόσο Alzheimer. Τα δύο χαρακτηριστικά της νόσου είναι οι τοξικές πλάκες β αμυλοειδούς που σχηματίζονται ανάμεσα στα εγκεφαλικά κύτταρα και τα νευροϊνιδικά πλέγματα πρωτεϊνών ταυ που μέσα στα κύτταρα.
Οι πλάκες β αμυλοειδούς σχηματίζονται από τα πρώιμα στάδια της νόσου Alzheimer, πριν καν οι πρωτεΐνες ταυ αρχίσουν να συσσωρεύονται.
Προηγούμενες έρευνες από την ίδια ομάδα ερευνητών είχαν δείξει ότι το φλεγμονόσωμα NLRP3 παίζει σημαντικό ρόλο στο σχηματισμό πλακών β αμυλοειδούς.
Η Σύνδεση Ανάμεσα στο Β Αμυλοειδές και την Ταυ
Εξετάζοντας συνολικά τα δεδομένα, οι επιστήμονες διαπίστωσαν ότι το φλεγμονόσωμα NLRP3 εμπλέκεται στο σχηματισμό τόσο των πλακών β αμυλοειδούς όσο και των νευροϊνιδικών πλεγμάτων της πρωτεΐνης ταυ.
«Τα αποτελέσματά μας υποστηρίζουν τη θεωρία του καταρράκτη αμυλοειδούς για την εμφάνιση της νόσου Alzheimer», είπε ο Heneka.
«Σύμφωνα με τη θεωρία αυτή, οι εναποθέσεις του β αμυλοειδούς οδηγούν τελικά σε εμφάνιση παθολογίας της ταυ και τελικά κυτταρικό θάνατο», εξήγησε.
Όπως τόνισε, το φλεγμονόσωμα αποτελεί πιθανώς το συνδετικό κρίκο ανάμεσα στο β αμυλοειδές και την ταυ. Ο Heneka και η ομάδα του ελπίζουν ότι οι παρατηρήσεις τους θα βοηθήσουν στην ανάπτυξη νέων θεραπειών που θα στοχεύουν τη διαδικασία μετατροπής της ταυ.
Συγκεκριμένα, υποστηρίζουν ότι είναι δυνατό να αναπτυχθούν φάρμακα που θα στοχεύουν την παθολογία της ταυ μέσω τροποποίησης της ανοσιακής απόκρισης.